拜耳避孕器安全性被严重质疑 未进入中国市场
近日,美国FDA可能大大低估了拜耳公司所生产的女性避孕器具Essure导致的致死事件数量,大量因Essure造成伤害的女性患者及其代表正在敦促FDA尽快做出决断,让Essure退出市场。
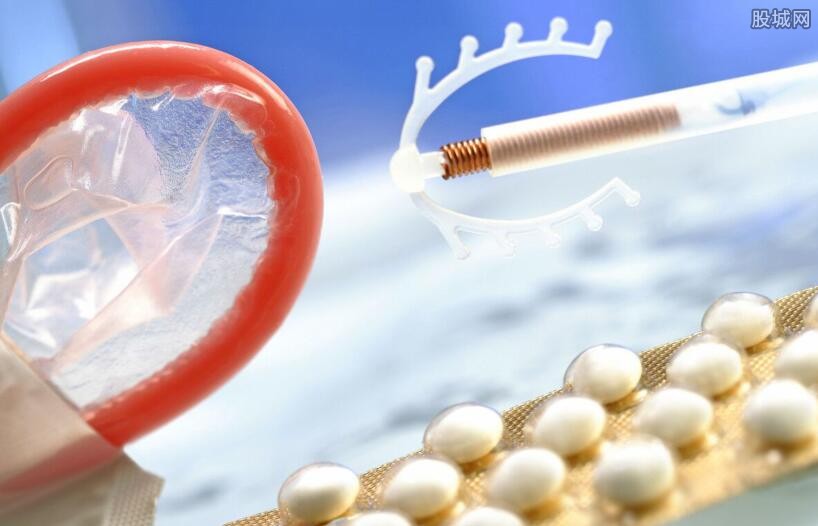
Essure是大型跨国药企拜耳公司研发并推出的女性避孕器具,是目前唯一一种经过美国FDA批准上市的非手术避孕器具,已进入市场13年。据拜耳Essure的官网介绍,Essure作为输卵管结扎的替代避孕方式,一旦植入女性体内,可达到永久性避孕,目前已被大约75万女性使用。
相关投诉达到万例:Essure安全性被严重质疑
其最大特点在于无需手术,只需将特殊材料制成的线圈借助导管经由阴道植入输卵管,线圈周围生成的组织形成卵子与精子接触的天然屏障,从而达到避孕目的。其植入过程通常仅需10分钟左右,在医生的诊室内即可完成,植入45分钟后即可回家,且医保可覆盖。拜耳声称,Essure可达到永久性避孕的效果,有效性高达99%以上。
然而,随着Essure被推广使用,越来越多疑似与Essure相关的不良事件或被患者投诉或被媒体报道出来。这些不良事件轻则涉及会产生疼痛、不适、阴道出血、晕厥等,重则涉及因器械在体内断裂引起的输卵管被刺穿、子宫出血等,甚至引起致死和意外怀孕。有些女性患者因为Essure在体内断裂游移,产生了并发症,不得不实施手术将断裂的残片取出。
有报道指出,FDA目前已收到近10000例有关Essure的投诉,其中包括303例致死事件。Essure的“受害者”还在社交网站“脸书”上建立了小组,专门用来分享Essure带来的健康损害,其成员目前已达到27000名。
Essure并未进入中国市场
2015年9月,鉴于针对Essure不良事件的投诉急剧增加,FDA召开了小组会议,由拜耳公司、患者及相关专家在会上进行举证和辩论。会议上,20名女性患者代表要求Essure退出市场。本月底,FDA即将做出是否要Essure撤市的决策。
对于患者代表对Essure的“弹劾”,拜耳公司表现强硬,坚称Essure“安全且有效”。拜耳Essure官网提到,Essure并非适用于所有女性,声称该产品对21岁以下和45岁以上女性的安全性和有效性尚无定论。
网站还在“重要安全信息”中指出,植入Essure前,需先确认过去6周内是否有过妊娠史或正在妊娠,输卵管是否已结扎以及近期是否患过盆腔炎,是否正在使用免疫抑制药物,对Essure所使用的材质是否有相关过敏史等。在植入Essure后的一段时间内,还要同时使用其他辅助避孕措施,直到医生评估Essure植入良好并起效后才可完全依赖Essure避孕。
在网站上,拜耳公司提示,Essure上市前的使用调查中,一些女性使用者在植入后会出现轻度至中度疼痛。罕见案例中,Essure可能发生断裂的情况。拜耳同时强调“没有一种避孕方法是100%有效的。植入Essure的女性发生宫外孕等异常妊娠的几率可能更高。”
尽管拜耳公司并不否认Essure的确会导致部分不良事件的发生,但对于“303例致死案例”这一数字并不认同,并于近日发表声明称这种“指控”是“不负责任的”。
据了解,Essure的75万使用者主要集中在美国。拜耳(中国)有限公司医药保健企业传播部相关人员对记者表示,中国市场并未引进过Essure,且以后也不会引进。